hemofilia
Synonimy
Hemofilia, dziedziczne zaburzenia krzepnięcia krwi, niedobór czynnika krzepnięcia krwi,
Niedobór czynnika VIII, niedobór czynnika IX, hemofilia
definicja
Hemofilia to dziedziczna choroba układu krzepnięcia krwi:
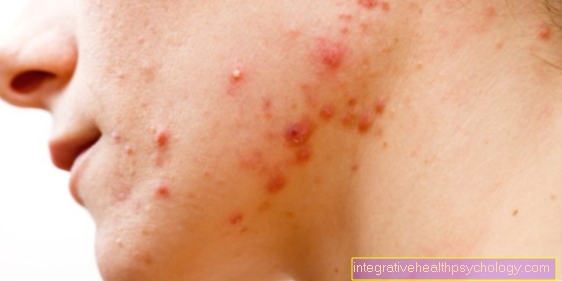
Pacjenci dotknięci chorobą mają zaburzenia krzepnięcia krwi, co objawia się tym, że krwawienie występuje przy najmniejszym urazie, a krwawienie jest trudne do zatrzymania.
Nie można aktywować czynników krzepnięcia, przez co nie jest możliwy regularny przebieg kaskady koagulacji.
Hemofilia to wrodzona choroba, która występuje w dwóch postaciach:
Mogą występować hemofilia A i B.
Hemofilia A występuje częściej (w 85% przypadków) niż postać B (ok. 15%) i jest poważniejszą z dwóch postaci.
Aktywność kompleksu czynnika VIII jest ograniczona w hemofilii A, ponieważ tworzenie się czynnika VIII-C w komórkach wątroby jest ograniczone.
Czynnik VIII-C jest jedną z dwóch podjednostek kompleksu czynnika VIII: von-Willebrand-Czynnik i czynnik VIII-C tworzą ten wspomagający krzepnięcie kompleks w kaskadzie krzepnięcia. Czynnik von Willebranda chroni czynnik VIII-C przed zbyt szybkim rozkładem.
W konsekwencji ilość funkcjonalnego kompleksu czynnika VIII zmniejsza się w postaci A.
w hemofilia B. synteza czynnika krzepnięcia IX zachodzi w mniejszym stopniu, przez co nie ma jego wpływu na proces krzepnięcia i zaburzona jest hemostaza.
Występowanie / epidemiologia
Występowanie hemofilii w populacji dotyczy hemofilii typu A. 1 na 5000 i dla formularza B. 1:15.000.
Fakt, że szczególnie mężczyźni chorują, wynika z problemów związanych z płcią
Związana z chromosomem X dziedziczenie defektu krzepnięcia (patrz przyczyna / rozwój).
Podstawy
Krzepnięcie krwi to precyzyjnie dostrojony system: różne składniki krwi, tak zwane czynniki krzepnięcia, są aktywowane jeden po drugim w sposób kaskadowy, aby umożliwić hemostazę w przypadku urazu.
Układ krzepnięcia składa się z pierwotnej i wtórnej hemostazy, zwanej również koagulacją plazmatyczną.
Jeśli ściana naczynia jest uszkodzona, dotknięte naczynie zwęża się w pierwszym kroku (= koagulacja pierwotna). Następnie rekwizyt (=Skrzeplina płytek krwi) w miejscu zranienia pokrytym płytkami krwi (= Płytki krwi) jest uformowana w celu uzyskania wstępnego uszczelnienia naczynia.
Powstanie skrzepliny aktywuje koagulację plazmastyczną:
Rozpoczyna się kaskada krzepnięcia, a interakcja różnych czynników krzepnięcia tworzy stabilną ranę lub zamknięcie naczynia.
Przyczyna i pochodzenie
Plik hemofilia Obie formy hemofilii są dziedziczone jako recesywna cecha sprzężona z chromosomem X.
W tak zwanym trybie dziedziczenia hemofilii sprzężonym z chromosomem X, informacja genetyczna produktu genowego dotyczy chromosomu X płci, który występuje w podwójnych liczbach u kobiet i pojedynczych liczbach u mężczyzn.
Każda informacja genetyczna ma dwa geny, tak zwane allele. Jeśli istnieje dziedziczenie recesywne, mutacja musi mieć wpływ na oba allele, aby wywołać chorobę: Recesywny oznacza, że patologicznie zmieniona informacja genetyczna pochodzi od zdrowego, tj. nie zmienia się, informacja jest tłumiona i nie prowadzi do choroby. Recesywna choroba dziedziczna rozwija się tylko wtedy, gdy oba allele zawierają nieprawidłową informację genetyczną.
Jest tylko za Chodź, zmieniła się ekspresja genu Nie do hemofilia.
Informacje: dziedziczenie
Jeśli tylko jedna ekspresja genów zostanie zmieniona, nie będzie choroby.
Ponieważ mężczyźni mają tylko jeden chromosom X w parze chromosomów płci, a zatem informacje o produktach genowych na ich chromosomie X są dostępne tylko w prostej formie, zachorują, jeśli tylko jeden allel jest uszkodzony.
Z drugiej strony kobiety, które mają dwa chromosomy X jako chromosomy płciowe, chorują tylko wtedy, gdy oba chromosomy mają wadliwe geny produktu genowego.
U mężczyzn cierpiących na hemofilię allel, który przenosi informacje dziedziczne dla czynnika krzepnięcia VIII-C (hemofilia A) lub czynnika krzepnięcia IX (hemofilia B) jest dostępny tylko w nieznacznie zmodyfikowanej postaci;
Kobiety muszą przenosić tę zmianę genetyczną na obu allelach, aby chorować.
Jeśli kobiety mają wadliwy i niezmieniony allel, nazywa się je nosicielkami dziedzicznej choroby sprzężonej z chromosomem X, takiej jak hemofilia.
W przypadku hemofilii nieprawidłowa informacja genetyczna skutkuje zmniejszeniem aktywności danego czynnika krzepnięcia lub zmniejszeniem produkcji czynnika krzepnięcia.
Chromosom X jest nośnikiem materiału genetycznego dla czynników krzepnięcia dla wtórnej hemostazy.
Około. 70% mutacji w materiale genetycznym powodujących hemofilię jest przenoszonych w rodzinach, 30% chorób wynika ze spontanicznych zmian (= spontanicznych mutacji) w informacji genetycznej.
diagnoza
Po zapytaniu o historię choroby pacjenta i dokładnym badaniu fizykalnym, są dodatkowe kroki w diagnostyce hemofilii:
W 2/3 przypadków w rodzinie występują przypadki hemofilii, dlatego też rodzinne zgrupowanie choroby należy zapytać, czy pacjent zgłosi się do lekarza z objawami podejrzanymi o hemofilię.
Pacjenci zgłaszają siniaki w wyniku najmniejszych urazów.
Jeden to rozróżnia Ciężkość hemofilii w łagodną, umiarkowaną lub ciężką postać choroby.
Badanie próbki krwi daje następujące wyniki typowe dla hemofilii:
Czas krwawienia jest normalny (= koagulacja pierwotna jest nienaruszona), ale funkcja koagulacji plazmatycznej jest ograniczona, dlatego tzw. Czas PTT jest dłuższy.
PTT oznacza czas częściowej tromboplastyny. Jest mierzony w badaniach laboratoryjnych w celu sprawdzenia funkcji czynników I, II, V, VIII do XII oraz XIV i XV.
Ponieważ w hemofilii brakuje jednego czynnika w kaskadzie krzepnięcia, nie może on działać w optymalny sposób, co skutkuje wydłużeniem czasu krzepnięcia.
Aby móc rozróżnić hemofilię A i B, krew pacjenta musi zostać zbadana pod kątem czynników VIII i IX; brak tych dwóch czynników decyduje o typie hemofilii.
Diagnostyka różnicowa
Hemofilię należy odróżnić od innych zaburzeń układu krzepnięcia, ze szczególnym uwzględnieniem zespołu von Willebranda-Jürgensa.
Czynnik von Willebranda (vWF) działa razem z czynnikiem VIII-C im
Kompleks czynnika VIII i powoduje zahamowanie przedwczesnej degradacji czynnika VIII, ponadto czynnik sprzyja krzepnięciu poprzez pośredniczenie w adhezji płytek krwi do uszkodzonego miejsca naczyniowego. Zatem vWF jest ważną częścią zarówno koagulacji pierwotnej, jak i wtórnej.
Jeśli występuje zespół von Willebranda-Jürgensa, wówczas powstanie
VWF w komórkach ściany naczynia zachodzą tylko w niewielkim stopniu lub w nieprawidłowy sposób. Obniżony poziom edukacji lub nieodpowiednia funkcja
Czynnik von Willebranda jest spowodowany mutacjami w genie odpowiedzialnym za tworzenie czynnika. Dziedziczenie zespołu lub wywołującej mutację genów jest dziedziczone w sposób autosomalny dominujący: informacja genetyczna dla vWF znajduje się na chromosomie numer 12, który nie jest chromosomem płci. W dominującym sposobie dziedziczenia chory allel hamuje działanie drugiego, zdrowego allelu, tak że choroba jest spowodowana mutacją genu i powoduje objawy kliniczne.
Pacjenci zwykle cierpią na krwawienie ze skóry i błon śluzowych, rzadziej na samoistne krwawienie, jak pacjenci z hemofilią.
Choroba jest często zauważana tylko wtedy, gdy po operacji występuje przedłużające się krwawienie.
Czas krwawienia u pacjenta po urazie ulega wydłużeniu, a wartości krzepnięcia osocza ulegają patologicznym zmianom (wydłużenie PTT).
Zespół von Willebranda-Jürgensa jest spowodowany podaniem desmopresyny lub substytucją czynnika VIII i vWF w celu ustabilizowania krzepnięcia (bardziej szczegółowe wyjaśnienie znajduje się w rozdziale „Leczenie hemofilii”).
Jakie są objawy hemofilii?
Objawy w postaci hemofilii nie różnią się:
- Hemofilia zwykle prowadzi do objawów klinicznych tylko u mężczyzn.
- Nadmierne krwawienie występuje przy hemofilii, co nie ma związku z poprzednim, w większości banalnym, przypadkiem (uraz), czas krwawienia jest normalny, ale zwykle występuje krwawienie, które nie występuje u osób zdrowych.
- Można wyróżnić trzy formy hemofilii, które są definiowane przez resztkową aktywność dotkniętych nią czynników krzepnięcia:
1.ciężka hemofilia (hemofilia) z mniej niż 1% resztkowej aktywności lub z częścią czynnika czynnościowego wciąż obecnego, w którym występuje samoistne krwawienie i występuje krwawienie do stawów
2. Umiarkowana hemofilia (choroba krwi) z aktywnością czynników wahającą się pomiędzy
1 i 5% normalnej aktywności czynnika i pojawienie się siniaków (= krwiaków) po niewielkich urazach
3. łagodna hemofilia (hemofilia), w którym nadal występuje aktywność szczątkowa 5-15% i w którym pacjenci zgłaszają objawy, takie jak krwiaki (siniaki) po znacznym urazie i krwawieniu pooperacyjnym.
Przeczytaj więcej na ten temat: Jakie są przyczyny krwotoku mózgowego
- Kobiety, które zwykle mają tylko zmienione informacje genetyczne dotyczące hemofilii, zwykle nie wykazują objawów klinicznych z ponad 50% resztkową aktywnością.
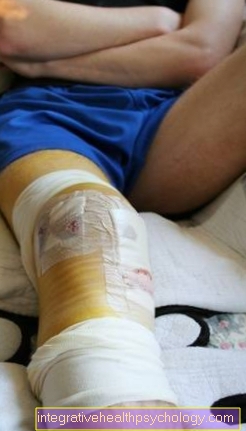
- Pacjenci doświadczają takich krwawień do dużych stawów kolano-, Cześć p- lub Staw barkowy, gdzie mówi się o hemartrozie. Krwawienie wywołuje reakcję zapalną z procesami naprawczymi w stawie, co może prowadzić do usztywnienia stawu.
- Może również krwawić do Muskulatura i przychodzą tkanki miękkie. Krwawienie prowadzi do wzrostu ciśnienia w mięśniach lub tkankach, ponieważ jest teraz większa objętość. Może to szczególnie wpłynąć na twoje ręce i nogi Zespół przedziału prowadzić:
Podwyższone ciśnienie powoduje ucisk naczyń krwionośnych i nerwów, przez co kończyny są niedostatecznie zaopatrzone i duże obszary tkanki mogą obumrzeć. Chirurg musi jak najszybciej leczyć zespół ciasnoty, aby zapobiec utracie kończyny. - Dochodzi do krwawienia do jamy brzusznej, co jest sytuacją zagrażającą życiu pacjenta.
- Po operacji możliwe jest niezwykle długotrwałe krwawienie.
Ponadto mogą występować długie okresy z krwią w moczu. Tutaj grozi Niedokrwistośćponieważ pacjent stale traci krew, prawdopodobnie niezauważoną. - Są szczególnie niebezpieczne Krwotok mózgowy (= krwawienie wewnątrzczaszkowe), które prowadzi do śmierci 10% osób z hemofilią. Więcej na ten temat można dowiedzieć się w naszym temacie Krwotok mózgowy.
Jak przebiega terapia hemofilii?

U chorego powinno wystąpić krwawienie hemofilia należy ich unikać, dlatego pacjent tego nie robi Lek które hamują krzepnięcie krwi, np Kwas acetylosalicylowy (Aspirin®) i bez iniekcji domięśniowych (= strzykawki do Muskulatura) odpowiednio.
Jeśli dojdzie do urazu z krwawieniem, bardzo ważna jest ostrożna miejscowa hemostaza, aby zapobiec krwawieniu do sąsiedniej tkanki.
Terapia lekowa hemofilia polega na zastąpieniu czynników krzepnięcia, których organizm nie jest w stanie wytworzyć w wystarczających ilościach.
Pacjenci z lekkim hemofilia w razie potrzeby otrzymać preparaty czynnika krzepnięcia, tj. jeśli wystąpił uraz z krwawieniem lub planowany jest poważny zabieg chirurgiczny, który może spowodować obfite krwawienie.
Profilaktyczną substytucję czynnika należy stosować u pacjentów z umiarkowaną do ciężkiej hemofilią, tj. brakujący czynnik należy podać na stałe, przed pojawia się krwawienie.
W przypadku resztkowej aktywności czynnika VIII powyżej 15% lub czynnika IX powyżej 20–25% regularne leczenie nie jest konieczne; pacjenci ci otrzymują brakujący czynnik krzepnięcia w przypadku samoistnego krwawienia lub przed planowanym zabiegiem chirurgicznym.
Terapia długoterminowa, jak i przed operacjami może odbywać się w postaci samodzielnego leczenia domowego, w którym pacjent samodzielnie aplikuje brakujący czynnik krzepnięcia.
Istnieje alternatywa terapii dla pacjentów z łagodną hemofilią:
Substancja czynna Desmopresyna (np. Minirin®) prowadzi do dystrybucji pliku
Czynnik VIII, który jest przechowywany w ścianach naczynia.
Lek można jednak podawać jednorazowo tylko przez kilka dni, ponieważ po pobudzeniu uwalniania czynnika pamięć w ścianach naczynia wyczerpuje się i trzeba ją ponownie odtworzyć.
W terapii ostrej hemofilia istnieją trzy możliwości interwencji:
- Pacjent otrzymuje aktywowaną protrombinę, substancję sprzyjającą krzepnięciu krwi, dzięki czemu krew zostaje zatrzymana tak szybko, jak to możliwe.
- Inną opcją terapeutyczną jest podawanie preparatów czynnika VII. Czynnik ten występuje na początku kaskady krzepnięcia i inicjuje jej regularny przebieg.
- Trzecią opcją terapeutyczną jest podanie zwierzęcego czynnika VIII-C w celu zatrzymania krwawienia.
Komplikacje
Prezent zastępczy (=podstawienie) czynników krzepnięcia może prowadzić do powstania przeciwciał przeciwko właśnie tym czynnikom, tak że podstawienie w stałej dawce nie ma już skutków terapeutycznych, dlatego mówi się o powstawaniu inhibitorów.
W zależności od oznaczenia stężenia przeciwciał we krwi pacjenta można podawać wysokie dawki czynnika VIII, których celem jest odzyskanie tolerancji na ten czynnik i wyłączenie powstawania przeciwciał. Zabieg ten powinien być wykonywany tylko w wyspecjalizowanych ośrodkach.
Istnieje niskie ryzyko zachorowania na zapalenie wątroby lub zakażenie wirusem HIV (=HIV), ponieważ czynniki pochodzą z produktów z krwi ludzkiej.
Innym ryzykiem leczenia substytucyjnego w przypadku hemofilii jest występowanie reakcji alergicznych.




.jpg)

.jpg)